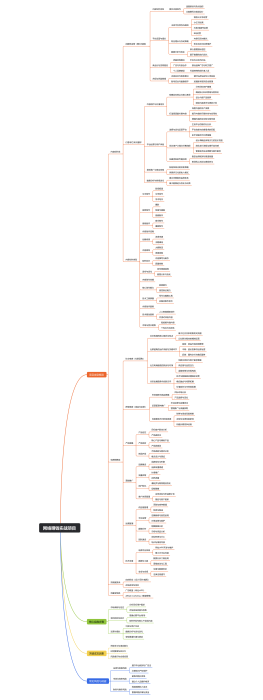
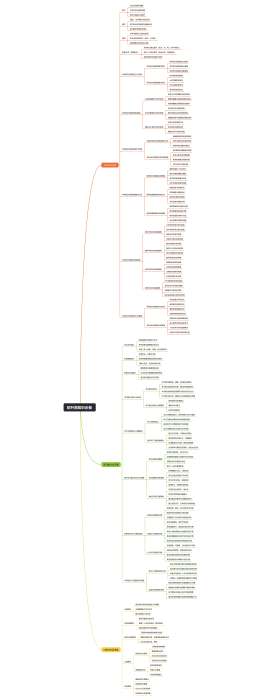
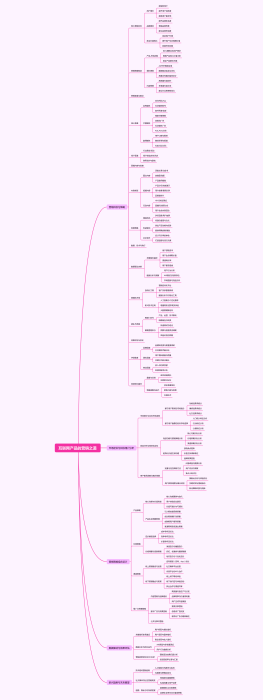
初中化学必考方程式总结
2025-07-22 21:46:36 0 举报
AI智能生成
初中化学必考方程式总结
模板推荐
作者其他创作
大纲/内容
0 条评论
下一页