细胞治疗双轨监管体系主要法规适用汇总
2024-01-11 10:44:23 0 举报
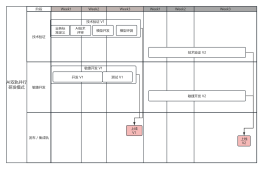
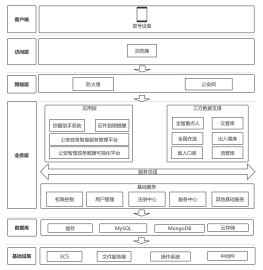
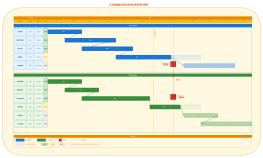
细胞治疗双轨监管体系主要法规适用汇总,这份文件概述了中国细胞治疗双轨监管体系的核心法规和适用范围。文件中详细介绍了细胞治疗产品的研发、注册、生产、流通和临床使用等方面的监管要求,以及双轨监管体系的特点和优势。这份文件对于了解中国细胞治疗行业的监管框架和政策环境具有重要的参考价值。
模板推荐
作者其他创作
大纲/内容
0 条评论
下一页