高中化学必修一
2022-08-03 20:10:05 4 举报AI智能生成
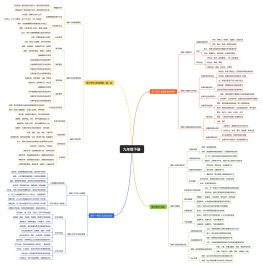
人教版高中化学必修一全书知识框架图
化学
化学必修一
高中化学必修一
高中化学
学习笔记
学校教育
模板推荐
作者其他创作
大纲/内容
第一章:从实验学化学
常见仪器的识别及用途
反应容器
直接加热:试管、蒸发皿、坩埚、燃烧匙
间接加热:烧杯、烧瓶(需垫上石棉网)
计量仪器
托盘天平、量筒
存取仪器
取固体:药匙、镊子
取液体:胶头滴管
存气体:集气瓶
存液体:细口瓶
存固体:广口瓶
基本实验操作
药品的取用
取用原则:三不原则,药品用量(取少量),用剩药品的处理,意外事故的处理
基本操作
药品的取用:块状或大颗粒、粉末状固体、液体
药品的称量或量取:量筒和托盘天平的使用,误差分析
物质的加热:酒精灯的使用方法,固体与液体的加热方法
装置气密性的检查
浓硫酸的稀释
过滤:主要仪器、装置及注意事项
蒸发:装置、注意事项
仪器的洗涤:洗涤方法,洗涤标志
药品的存放
易氧化:隔绝空气保存(如金属钠、白磷)
易吸水、挥发或潮解:密封保存(如浓硫酸、浓盐酸、氢氧化钠固体)
见光易分解或变质:棕色瓶避光保存(如硝酸、硝酸银)
第二章:化学物质及其变化
物质的分类
纯净物和混合物
纯净物
由一种物质组成的,纯净是相对的,绝对纯净的物质是没有的,只要杂质含量低,不至于对生产和科学研究产生影响的物质就是纯净物
混合物
由两种或多种物质组成,这些物质相互间没有发生化学反应,各物质都保持各自的性质(例如:空气、雨水、溶液、碳酸饮料、牛奶等)
划分纯净物、混合物的标准是根据物质的种类来划分的
物质的组成
从宏观的角度看,物质由元素组成的;
物质组成的判断依据
根据有无固定的组成或有无固定的熔沸点可判断该物质是纯净物还是混合物
对于化合物可根据晶体类型判断:离子晶体是由阴/阳离子构成的;分子晶体是由分子构成的;原子晶体是由原子构成的
对于单质也可根据晶体类型判断:金属单质是由金属阳离子和自由电子构成的;原子晶体、分子晶体分别由原子、分子构成
物质的分类
常见的分类方式
交叉分类法
依据不同的分类标准,对同一事物进行多种分类的种分类方法
树状分类法
对同类事物按照某些属性进行再分类的分类法
分散系及其分类
概念
把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。其中被分散的物质称为分散质,起容纳分散质作用的物质称为分散剂
分类
按照分散质或分散剂的状态(气、液固)共分为九种分散系
按照分散质粒子的大小将分散系分为溶液(小于1 nm),胶体(1 ~ 100 nm)和浊液(大于100 nm)
胶体
定义
分散质粒子直径介于1 ~ 100 nm之间的分散系
分类
按分散剂的状态可将胶体分为固溶胶(如烟水晶);液溶胶如Fe(OH)₃;和气溶胶(如雾云、烟)
胶体的性质及应用
胶体可发生于达尔效应、布朗运动、电泳和聚沉等
物质的简单分类及其依据
氧化物及其分类
金属氧化物
Na₂O、MgO、Al₂O₃、Na₂O₂、Fe₃O₄
非金属氧化物
CO、CO₂、NO、NO₂、SO₂、SO₃、H₂O、H₂O₂
酸及其分类
无氧酸
H₂S、HF、HCl、HBr、HI、HCN
含氧酸
H₂CO₃、HNO₃、H₃PO₄、H₂SO₄、H₂SiO₃、HClO
强酸
HCl、HBr、HI、H₂SO₄、HNO₃、HClO₄
弱酸
H₂CO₃、H₂SO₃、HClO、CH₃COOH、H₃PO₄、H₂S、HF、HCN
碱及其分类
一元碱
NaOH、KOH、NH₃·H₂O
二元碱
Ca(OH)₂、Ba(OH)₂
多元碱
Fe(OH)₃
强碱
NaOH、KOH、Ca(OH)₂、Ba(OH)₂
弱碱
NH₃·H₂O及难溶性碱
盐的分类
依据阳离子的种类
钠盐、钾盐、铵盐等
依据酸根离子
盐酸盐、碳酸盐、硫酸盐、硝酸盐
依据酸碱中和程度
酸式盐
NaHCO₃、NaHCO₄、NaH₂PO₄、Na₂HPO₄
碱式盐
Cu₂(OH)₂CO₃
离子反应
概念
电离
对象
电解质
分类:酸、碱、盐、金属氧化物、水
溶液导电
实质
反应物的某些离子浓度的减小
发生条件
生成沉淀、气体、弱电解质
类型
氧化还原反应
非氧化还原反应
离子方程式
概念
用实际参与反应的离子符号表示离子反应的式子
意义
表示同一类型的反应
书写步骤
写拆删查
不拆的物质口诀:弱非难溶氧气单
常见问题
判断离子方程式正误
与量有关的离子方程式
口诀:谁少谁为1
离子共存
一色
有色离子
Cu²⁺(蓝色)、Fe²⁺(浅绿色)、Fe³⁺(棕黄色)、MnO₂(紫红色)
二性
溶液的酸碱性
酸性下:OH⁻、CO₃²⁻、HCO₃⁻、HSO₃⁻、SO₃²⁻、CH₂COO⁻不能大量存在
碱性下:H⁺、HCO₃⁻、HSO₃⁻、NH₄⁺、AI³⁺、Mg²⁺、Fe³⁺等不能大量存在
三特殊
AIO₂⁻与HCO₃⁻不能大量共存
NO₃⁻与H⁺组合具有强氧化性,不能与SO₃²⁻、Fe³⁺、I⁻等共存
四反应
复分解反应
如生成沉淀、气体、弱电解质则不能共存
氧化还原反应
如Fe²⁺与I⁻
生成配合物的反应
如Fe³⁺与SCN⁻
氧化还原反应
实质
电子的转移
特征
化合价的升降
口诀
升失氧,降得还
类型
一般氧化还原:如二氧化锰和浓盐酸制氯气
歧化反应:如氯气和水反应
归中反应:如硫与浓硫酸的反应
电子的转移方法
单线桥
双线桥
三大律
守恒律
考察与n的结合的化学量,如eˉ,m,V,N,c
强弱律
氧化性
氧化剂>氧化产物
还原性
还原剂>还原产物
价态率
高价氧,低价还,中间两俱全,相邻价态不氧还,只靠拢不交叉
方程式配平
原则
电子守恒、电荷守恒、原子守恒
方法
标变价、找变化、求总数、配系数
第四章:非金属及其化合物
无机非金属材料的主角
二氧化硅SiO₂
存在
SiO₂的存在形式有结晶形和无定形两大类,水晶、玛瑙的主要成分是结晶的二氧化硅
结构
SiO₂晶体是由Si和O按原子数之比为1:2的比例组成的立体网状结构的晶体。每个硅原子周围结合4个O原子,每个O周围结合2个Si原子
物理性质
熔点高;硬度大;不溶于水
用途
①沙子是基本的建筑材料
②纯净的SiO₂是现代光学及光纤制品的基本原料,可以制作光导纤维
③石英和玛瑙制作饰物和工艺品
④实验室中使用石英坩埚
硅酸H₂SiO₃
物理性质
硅酸是一种难溶于水的白色胶状物
化学性质
弱酸性
向Na₂SiO₃溶液中通入CO₂,生成白色沉淀
Na₂SiO₃+CO₂+H₂O=Na₂CO3+H₂SiO₃↓
H₂SiO₃酸性比H₂CO₃酸性弱
不稳定性
H₂SiO₃不稳定,受热易分解
H₂SiO₃=加热=H₂O+SiO₂
制备
Na₂SiO₃溶液中加入盐酸
Na₂SiO₃+2HCl=2NaCl+ H₂SiO₃(胶体)
存在及用途
浓度小且边加边振荡时,形成硅酸溶胶(胶体);浓度大时,形成硅酸凝胶
硅胶
硅酸凝胶经干燥脱水得到的硅酸干凝胶,称为“硅胶”,具有很强的吸水性,常用作干燥剂或催化剂的载体
富集在海水中的元素
单质
物理性质
黄绿色有毒、有刺激性气味,密度比空气大,易液化称液氯,可溶于水
氯元素自然界以化合态存在(NaCl)
化学性质
与金属单质反应(生成最高价)
与非金属单质反应
与H₂O反应
与碱反应
漂白液
漂白粉
制备
原理
MnO₂+4HCI(浓)=加热=MnCl₂+CI₂↑+2H₂O
装置
产生装置
除杂装置
收集装置
尾气处理装置
化合物
氧化物
酸
HCl
酸性
HCIO
不稳定易分解
弱酸性,可使湿润石蕊试纸先变红后褪色
强氧化性
漂白性
Cl₂、HClO、H₂O(3分子)
H¯、Cl¯、ClO¯、OH¯(4离子)
HCIO₄
自然界中酸性最强的无机酸
硫和氮的氧化物
硫
硫单质
物理性质
淡黄色固体,难溶于水,可溶于酒精,易溶于CS₂,熔沸点都很低
化学性质
氧化性
与绝大多数金属反应
Fe+S=加热=FeS
2Cu+S=加热=Cu₂S
与非金属
H₂+S=加热=H₂S
H₂S是一种臭鸡蛋气味的有毒气体,有强还原性
还原性:与氧气发生反应
S+O₂=点燃=SO₂
硫在空气中燃烧发出淡蓝色的火焰,在氧气中燃烧发出蓝紫色的火焰
自身氧化还原反应
3S+6NaOH=2Na₂S+Na₂SO₃+3H₂O
SO₂的性质
物理性质
状态:气体
颜色:无色
气味:有刺激性
沸点:-10℃
毒性:有毒
密度:比空气大
溶解度:易溶于水,在常温、常压下,1体积水大约能溶解40体积的SO₂
化学性质
是一种重要的酸性氧化物,具有酸性氧化物的通性
与H₂O反应
SO₂+H₂O=H₂SO₃(亚硫酸,二元中强酸,只能存在于水中)
与碱反应
SO₂+2NaOH=Na₂SO₃+H₂O
SO₂+NaOH=NaHSO₃
与碱性氧化物的作用
SO₂+Na₂O=Na₂SO₃
与某些盐反应
SO₂+2NaHCO₃=Na₂SO₃+H₂O+2CO₂↑
SO₂可以被H₂O₂、Na₂O₂、HNO₃、O₃等多种强氧化剂所氧化
SO₂的污染
酸雨
空气中SOx和NOx随雨水下降成为酸雨,pH<5.6
SO₂的制备
Na₂SO₃+H₂SO₄=Na₂SO₄+SO₂↑+H₂O
收集方法
向上排空气法或排饱和NaHSO₃溶液
SO₂的鉴定
通入品红溶液褪色,加热后又恢复原色
湿润的蓝色石蕊试纸——变红
SO₂的干燥
浓H₂SO₄
吸收SO₂尾气
可选用酸性高锰酸钾溶液或碱液等
SO₂的用途
制H₂SO₄、漂白剂、杀菌、消毒
SO₃
物理性质
三氧化硫又名硫酸酐,是一种无色易挥发的固体,熔点16.83℃,沸点44.8℃
化学性质
H₂SO₄的酸酐;S元素为+6价,处于最高价态,只有氧化性
与水反应,放热
SO₃+H₂O=H₂SO₄
CaO+SO₃=CaSO₄
Ca(OH)₂+SO₃=CaSO₄+H₂O
工业上制取硫酸
S→SO₂→SO₃→H₂SO₄
SO₃+H₂O=H₂SO₄
SO₂和CO₂
分支主题
氮的循环
氮气
物性
氮的固定
自然固氮
生物固氮/高能固氮
人工固氮
合成氨/仿生固氮
与镁反应
重要氧化物
NO
物性
与O₂
NO₂
物性
与H₂O
氨气
物性
喷泉实验
化性
与H₂O/酸/催化氧化
铵盐
物性
化性
受热不稳定:NH₄HCO₃/NH₄CI
与碱反应
固态:实验室制氨气
溶液:离子反应
常温/加热
铵盐的检验
硝酸
物性
化性
强酸性
不稳定性
见光或受热分斛
强氧化性
金属:Al
Fe
Cu
硝酸根的检验
非金属:C
S
氮的氧化物溶于水的有关计算
讨论法
电子守恒法
硝酸与金属反应的计算规律
电子守恒
N守恒
溶液中电荷守恒
人类对环境的污染
大气污染:光化学烟雾/酸雨
水体污染:水体富营养化
氨 硝酸 硫酸
氨的性质
氨的固定
概念
将游离态的氨转变为氮的化合物
类型
①人工固氮
工业合成氨:N₂+3H₂↔2NH₃
②自然固氮
雷雨发庄稼
N₂+O₂=2NO
2NO+O₂=2NO₂
3NO₂+H₂O=2HNO₃+NO
③生物固氮
如豆科植物的根瘤苗能够将空气中的氮转化为含氮化合物而促进自身生长
④化学模拟生物固氮
利用化学方法模拟固氮酶的作用,在温和条件下将氮转变为氨
氨的物理性质
①颜色
无色
②气味
刺激性
③溶解性
极易溶于水(1:700)
④是否易液化
易液化
氨的化学性质
①与水反应
②与酸反应(呈现碱性)
③弱还原性
铵盐
概念
由NH₄⁺和酸根离子构成的化合物
物理性质
都是晶体,都易溶于水,常伴有吸热现象
化学性质
受热易分解
热分解情兄与对应的酸有关。一般非氧化性酸的铵盐热分解产物为NH₃与对应酸。氧化性酸的铵盐热分解比较复杂产物有N₂或其氧化物出现
NH₄NO₃=加热=N₂O↑+2H₂O
NH₄NO₂=加热=N₂↑+2H₂O
(NH₄)₂Cr₂O₇=加热=N2↑+Cr₂O₃+4H₂O
铵盐受热一会放出氨气,但不是都放出氨气。如NH₄NO₃受热到一定程度会发生爆炸,产生多种气体的混合气
与碱反应
铵盐会和强碱溶液在加热条件下反应生成NH₃
NH₄⁺+OH⁻=加热=NH₃ +H₂O
NH₄⁺的检验
实验操作
取侍捡物少许,向其中加入NaOH溶液,加热后若产生能使显润的红色石蕊试纸变蓝的气体,则一定含NH₄⁺
反应原理
NH₄⁺+OH⁻=加热=NH₃↑+H₂O
氨气的实验室制法
方法1:铵盐与碱共热
①原埋
NH₄CI与Ca(OH)₂固体共热产生氨:2NH₄Cl+Ca(OH)₂=CaCl₂+2NH3↑+2H₂O
②装置
“固+固”,加热型反应装置,包括试管、酒精灯等
③收集
氨气易溶于水,密度比空气
用向下排空气法收集
④检验
用湿润的红色石蕊试纸(变蓝)或蘸有浓盐酸的玻璃棒接近试管口(有白烟)
⑤棉花团的作用
防止试管内的NH₃与试管外的空气形成对流,以便收集到较为纯净的氨
⑥注意事项
不能用NH₄NO₃跟Ca(OH)₂反应制氨气
硝酸铵受撞击、加热易爆炸,且产物与温度有关,可能产生NH₃,N₂,N₂O,NO
不能用NaOH、KOH代替Ca(OH)₂
NaOH,KOH是强碱,具有吸湿性(潮解)易结块,不易与铵盐混合充分接触反应
KOH、NaOH具有强腐蚀性在加热情况下,对玻璃仪器有腐蚀作用
用试管收集氨气要堵棉花
NH₃分子微粒直径小,易与空气发生对流,堵棉花目的是防止;NH₃与空气对流,确保收集纯净的氨气;减少NH3对空气的污染
实验室制NH₃除水蒸气用碱石灰,而不采用浓H₂SO₄和固体CaCl₂
浓H₂SO₄与NH₃反应生成(NH₄)₂SO₄,NH₃与CaCl₂反应能生成CaCl₂·8NH₃(八氨合氯化钙)
CaCl₂+8NH₃= CaCl₂·8NH₃
方法2:浓氨水中加固态碱性物质
①原理
向浓氨水中加入固态碱性物质,消耗浓氨水中的水,同时反应放热,促进NH₃·H₂O分解产生氨
NH₃·H₂O=加热=NH₃↑+H₂O
固态碱性物质:CaO、NaOH、碱石灰等
②装置
“固+液”型反应装置
③收集、检验
方法3:加热浓氨水
原理
NH₃·H₂O=加热=NH₃↑+H₂O
硫酸
稀硫酸的性质—酸的通性
①紫色石蕊试液变红色,无色酚酞试液下变色
②与沽泼金属反应
③与碱性氧化物反应
④与碱反应
⑤与某些盐反应
浓硫酸的特性
①吸水性
①将一瓶浓硫酸敞口放置在空气中其质量将增加,密度将减小,浓度降低,体积变大
②干燥剂和洗气装置。浓硫酸可以干燥中性和酸性气体中性气体:CO、氧气、氮气和所有的稀有气体;酸性气体:HCl气体、二氧化碳、二氧化疏、氯气等
①浓硫酸不能用作碱性、性气体(例如氢气)的洗气转置,因为浓疏酸与氨气反应
②浓硫酸不可干燥溴化氢、碘化氢、硫化氢等还原性气体
③浓硫酸实际上不能干燥二氧化疏,因力二氧化硫易溶于浓硫酸
④硫酸不能干燥二氧化氮,因为NO₂溶于浓硫酸生成亚硝基硫酸等一些物质
②脱水性
按水的组成比脱去某些有机物中的氢、氧元素,使有机物脱水如使纸张、棉花、木材、蔗糖等有机物脱水炭化(变黑)
有水则吸,无水则脱
③强氧化性
①与绝大多数金属反应
冷的浓H₂SO₄使Fe、Al等金属钝化
②与非金属反应
硫酸的用途
①重要的化工原料和化学实验室中必备的重要试剂
②工业上制化肥、农药、炸药和染料等
③用于精炼石油、金属加工前的酸洗及制取各种挥发性酸等
SO₄²⁻的检验
①正确操作
待测液→盐酸酸化→取清夜→BaCl₂溶液→白色沉淀,即可确定存在硫酸根离子
②理论解释
①先加稀盐酸的目的是排除CO₃²⁻、SO₃²⁻、Ag⁺等离子的干扰
②再加BaCl₂溶液,有白色沉淀产生,BaSO₄既准溶于水,又难溶于酸
SO₄²⁻+Ba²⁺→BaSO₄↓
硝酸
化学性质
①具有酸的通性
①与指示剂作用
稀硝酸能使紫色石蕊试液由紫色变为红色
浓硝酸使紫色石蕊先变红(H⁺的作用)后褪色(强氧化性)
②与碱性氧化物反应
③与碱反应
④与某些盐反应
②不稳定性
①硝酸在受热或光照下易发生分解反应
硝酸越浓越容易分解
②浓硝酸呈黄色的原因
硝酸分解生成的NO₂溶解在硝酸中
③硝酸的保存
硝酸保存在棕色(防光)试剂瓶中,置于冷暗处,不能用橡胶塞(橡胶塞易被氧化)
③强氧化性
①与金属反应
HNO₃几乎能与所有的金属(除金、铂外)发生氧化还原反应,冷的浓硝酸使铁、铝发生钝化
②与非金属反应
③与某些还原物质反应
④氧化某些有机物
硝酸的用途
重要的化学原料和化学试剂,在工业上用于制化肥、农药、炸药和染料等
第三章:金属及其化合物
金属的化学性质
金属的概述
金属的存在
绝大多数:化合态
极少数:游离态,如:Pt、Au
金属的物理性质
共性
具有金属光泽
有良好的导电性、导热性和延展性
密度大
熔、沸点较高
特性
绝大多数金属是银白色,铜是紫色,金是黄色
绝大多数金属为固体,汞(俗称“水银”)常温下是液体
金属的化学通性
金属原子最外层电子较少,在化学反应中易失去电子,表现比较强的还原性
在化合物中只有正化合价,无负化合价,不同金属的活泼性不同
金属与非金属
大多数金属能与氧气反应生成相应的化合物
金属与酸
较活泼金属均可以与盐酸等发生置换反应,生成盐,放出氢气
金属与盐
有些金属可以失去电子,将盐中其他金属元素置换出来,表现还原性
金属的应用
金属的存在形态、金属的含量(富集过程)、金属的治炼的成本及金属制品的用途决定了金属元素被广泛应用。人类利用金属的历史经历了青铜器时代直至目前的金属合金时代
金属与非金属的反应
钠
钠与氧气
4Na+O₂=2Na₂O
2Na+O₂=加热=Na₂O₂
钠加热的现象
钠受热熔化成小球后剧烈燃烧,发出黄色火焰
生成淡黄色固体
钠与其他
2Na+S=加热或研磨=Na₂S
2Na+Cl₂=点燃=2NaCl
铝
铝与氧气
4Al+3O₂=点燃=2Al₂O₃
铝加热的现象
铝箔剧烈燃烧,发出耀眼的白光,瓶内充满大量白烟
铝与其他
2Al+3S=加热=Al₂S₃
2Al+3Cl₂=点燃=2AlCl₃
金属与酸和水的反应
钠
钠与水
步骤
在烧杯中加入一些水,滴加几滴酚酞溶液,然后把一小块钠放入水中
现象
浮
金属钠浮在水面上
钠的密度比水小
熔
金属钠熔化成闪亮的小球
该反应放热,钠的熔点低
游
钠在水面上四处游动
反应中产生气体
响
发出嘶嘶的响声
钠与水反应剧烈,生成气体
红
反应后的溶液呈红色
反应生成物中有碱性物质
反应式
2Na+2H₂O=2NaOH+H₂↑
实质:钠与水电离出的氢离子反应
2Na+2H₂O=2Na⁺+2OH⁻+H₂↑
钠与酸
2Na+2H⁺=2Na⁺+H₂↑
实质:钠与酸电离出的氢离子反应
铁与水蒸气
3Fe+4H₂O=加热=Fe₃O₄+4H₂
铁不能与冷水、热水反应,常温下,铁在潮湿的空气中容易生锈,实质是铁与水、氧气发生反应
铝
铝与酸
2Al+6HCl=2AlCl₃+3H₂↑
2Al+6H⁺=2Al³⁺+3H₂↑
铝与碱
2Al+2NaOH+2H₂O-2NaAlO₂+3H₂↑
2Al+2OH⁻+2H₂O=2AlO₂⁻+3H₂↑
几种重要的金属化合物
钠及其化合物
单质
物理性质
银白色,密度小,熔沸点低,硬度小
保存在煤油中
化学性质
非金属单质反应
与水反应
浮熔游响红
与酸反应
与盐溶液反应
与熔盐反应
氧化物
Na₂O
物理性质
白色固体
制备
Na在常温下与空气接触就可反应生成
化学性质
碱性氧化物
过氧化物
Na₂O₂
物理性质
淡黄色固体
制备
Na在空气中加热或与氧气在点燃条件下生成
化学性质
与水反应
与CO₂反应
钠及相关计算
单质的计算
钠与氧气反应计算
钠与水反应计算
钠与盐溶液反应
过氧化钠的计算
与Na₂O₂有关的N₂题
与质量相关的差量计算
Δm=28xnCO₂+2xnH₂
与体积相关的差量计算
nΔV:nCO₂或nH₂O:nO₂=1:2:1
碳酸钠、碳酸氢钠及相关计算
铝及其化合物
铝单质的性质
物理性质
银白色,较软的固体,导电、导热,具有良好的延展性
化学性质
与非金属
4Al+3O₂=点燃=2Al₂O₃
2Al+3Cl₂=加热=2AICl₃
与酸
Al+6HCl=2AICl₃+3H₂↑
2Al+3H₂SO₄=Al₂(SO₄)₃+3H₂↑
常温常压下,铝遇浓硫酸或浓硝酸会发生钝化,所以可用铝制容器盛装浓硫酸或浓硝酸
与强碱
2Al+2NaOH+2H₂O=2NaAlO₂(偏铝酸钠)+3H₂↑
大多数金属不与碱反应,但铝却可以
铝的化合物
氧化铝Al₂O₃
物理性质
白色固体、熔点高、不溶于水,不与水化合。常作耐火材料
化学性质
与酸
Al₂O₃+6H⁺=2Al³⁺+3H₂O
与碱
Al₂O₃+2OH⁻=2AlO₂⁻+H₂O
氢氧化铝Al(OH)₃
物理性质
白色胶状物质,不溶于水,有强的吸附性,可以吸附水中的悬浮物和各种色素
化学性质
不稳定性:氢氧化铝不稳定,受热易分解
实验室制备
AlCl₃+3NH₃·H₂O=Al(OH)₃↓+3NH₄Cl
Al³⁺+3NH₃·H₂O=Al(OH)₃↓+3NH₄⁺
与酸
AlO₂+H⁺=Al(OH)₃
与碱
Al³⁺+3OH⁻=Al(OH)₃
明矾KAl(SO₄)₂·12H₂O
复盐的概念
由两种不同的金属离子和一种酸根离子组成的盐叫复盐
KAl(SO₄)₂=K⁺+A1₃⁺+2SO₄²⁻
A1³⁺+3H₂O=加热=Al(OH)₃(胶体)+3H⁺
因为Al(OH)₃具有很强的吸附性,所以明矾可以做净水剂
A1³⁺和AlO₂⁻的性质
A1³⁺的性质
AlCl₃中逐滴加入氨水
Al³⁺+3NH₃·H₂O=Al(OH)₃↓+3NH₄⁺
Al³⁺制取Al(OH)₃用弱碱更合适
AlCl₃中逐滴加入NaOH溶液至过量
方程式
Al³⁺+3OH⁻=Al(OH)₃
Al₂O₃+OH⁻=AlO₂⁻+2H₂O
现象
白色沉淀先增加再减少最后消失
向NaOH溶液中滴加AlCl₃
方程式
Al³⁺+4OH⁻=AlO₂⁻+2H₂O
Al³⁺+3AlO₂⁻+6H₂O=4Al(OH)₃↓
AlO₂⁻的性质
向含有AlO₂⁻的偏铝酸盐溶液中通入CO₂直至过量
2AlO₂⁻+CO₂(少量)+3H₂O=2Al(OH)₃↓+CO₃²⁻
AlO₂⁻+CO₂(足量)+2H₂O=Al(OH)₃↓+HCO₃⁻
向含有AlO₂⁻的偏铝酸盐溶液中逐滴滴入稀盐酸直至过量
AlO₂⁻+H⁺+H₂O=A1(OH)₃↓
A1(OH)₃+3H⁺= Al³⁺+3H₂O
向含有H⁺的强酸溶液中逐滴滴入偏铝酸盐溶液直至过量
AlO₂⁻+4H⁺= Al³⁺+2H₂O
Al³⁺+3AlO₂⁻+6H₂O=4Al(OH)₃↓
铁及其化合物
单质铁
性质
物理性质
铁片是银白色,铁粉是黑色
化学性质
与非金属单质
3Fe+2O₂=点燃=Fe₃O₄
现象:剧烈燃烧,火星四射,生黑色的固体
2Fe+3Cl₂=点燃=2FeCl₃
Fe+S=加热=FeS
与非氧化性酸
Fe+2HCl=FeCl₂+H₂↑
Fe+2H⁺=Fe²⁺+H₂↑
常温下铝、铁遇浓硫酸或浓硝酸钝化。加热能反应但无氢气放出
与盐溶液
Fe+CuSO₄=FeSO₄+Cu
Fe+Cu²⁺=Fe²⁺+Cu
铁与水蒸气
反应现象:加热时试管内铁粉红热,点燃肥皂泡可听到爆鸣声
3Fe+4H₂O=高温=Fe₃O₄+4H₂↑
铁的氧化物
FeO、Fe₂O₃、Fe₃O₄
物理性质
氧化亚铁FeO
黑色粉末
铁+2价
氧化铁Fe₂O₃
红棕色粉末
铁+3价
四氧化三铁Fe₃O₄
黑色晶体
铁+2、+3价
化学性质
不溶于水也不与水反应
与酸反应
FeO+2H⁺=Fe²⁺+H₂O
Fe₂O₃+6H⁺=2Fe³⁺+3H₂O
Fe₃O₄+8H⁺=2Fe³⁺+Fe²⁺+4H₂O
FeO不稳定易氧化
均能被CO还原成Fe
铁的氢氧化物
Fe(OH)₃、Fe(OH)₂
制备
Fe(OH)₃
Fe³⁺+3OH⁻=Fe(OH)₃↓
产生红褐色沉淀
Fe(OH)₂
Fe²⁺+2OH⁻=Fe(OH)₂↓
生成白色沉淀,迅速变为灰绿色,最后变成红褐色
化学性质
Fe(OH)₂+2H⁺=Fe²⁺+2H₂O
Fe(OH)₃+3H⁺=Fe³⁺+3H₂O
2Fe(OH)₃=加热=Fe₂O₃+3H₂O
铁盐和亚铁盐的鉴别
Fe³⁺
溶液呈棕黄色
加碱液
Fe³⁺+3OH⁻=Fe(OH)₃↓产生红褐色沉淀
加KSCN溶液
Fe³⁺+3SCN⁻=Fe(SCN)₃呈现血红色
Fe²⁺
溶液呈浅绿色
加碱液
Fe²⁺+2OH⁻=Fe(OH)₂↓产生白色沉淀
4Fe(OH)₂+O₂+2H₂O=4Fe(OH)₂产生红褐色沉淀
白色沉淀迅速变为灰绿色,最后变成红褐色
加KSCN溶液
Fe³⁺+3SCN⁻=Fe(SCN)₃
将Fe²⁺转化为Fe³⁺
Fe²⁺加KSCN溶液,加氯水
评论
0 条评论
下一页