体细胞临床研究工作指引
2025-09-18 21:28:41 0 举报
AI智能生成
体细胞临床研究工作指引 思维导图,总结体细胞临床研究工作指引要求内容,方便企业参考制定总结相关申报文件
模板推荐
作者其他创作
大纲/内容
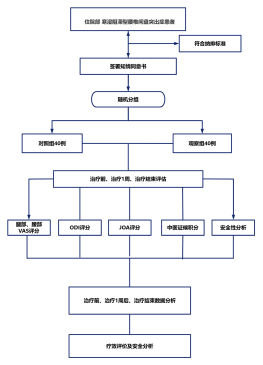
Collect
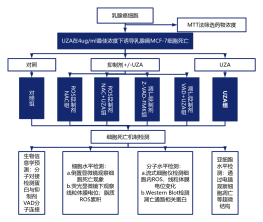
Collect
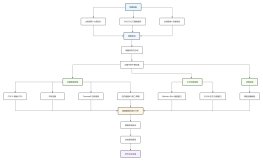
Collect

Collect
0 条评论
下一页


