
医疗器械相关法律法规系统
2022-10-28 18:50:16 3 举报AI智能生成
医疗器械相关法律法规系统是指国家为了保障人民群众的生命健康安全,规范医疗器械的生产、经营、使用和监督管理而制定的一系列法律法规。这些法律法规包括《医疗器械监督管理条例》、《医疗器械注册管理办法》、《医疗器械生产质量管理规范》等。这些法律法规旨在加强对医疗器械的管理,保证医疗器械的安全有效,维护人民群众的合法权益。同时,这些法律法规也为从事医疗器械相关业务的企业和个人提供了明确的指导和依据。
医疗器械
法规
法规体系
行业监管
模板推荐
作者其他创作
大纲/内容
【上市前注册】
【注册与备案】
《医疗器械注册与备案管理办法》<br>国家市场监督管理总局令第47号 2021.10.01施行<br>
关于实施《医疗器械注册与备案管理办法》《体外诊断试剂注册与备案管理办法》<br>有关事项的通告(2021年第76号)2021.09.29
【注册资料】
关于公布医疗器械注册申报资料要求和批准证明文件格式的公告<br>(2021年第121号)2022-01-01执行<br>
中华人民共和国医疗器械注册证(格式)
中华人民共和国医疗器械变更注册(备案)文件(格式)
国家药品监督管理局医疗器械临床试验审批意见单(格式)
医疗器械注册申报资料和批准证明文件格式要求
医疗器械注册申报资料要求及说明
医疗器械延续注册申报资料要求及说明
医疗器械变更备案/变更注册申报资料要求及说明
变更备案
变更注册
医疗器械临床试验审批申报资料要求及说明
医疗器械安全和性能基本原则清单
《医疗器械安全和性能的基本原则》<br>2020年第18号通告<br>
国家药监局器审中心关于发布医疗器械安全和性能基本原则符合性技术指南的通告<br>(2022年第29号)2022-07-13<br>
关于发布医疗器械注册电子申报目录文件夹结构的通告<br>(2021年第15号)2021.11.15<br>
国家药监局关于医疗器械主文档登记事项的公告<br>(2021年第36号)2021-03-12<br>
1.医疗器械主文档登记申请表
2.医疗器械主文档登记更新申请表
3.医疗器械主文档登记回执
4.医疗器械主文档登记相关信息
5.医疗器械主文档登记资料形式要求
6.医疗器械主文档登记相关事项说明
【审评审批】
国家药监局关于印发境内第二类医疗器械注册审批操作规范的通知<br>国药监械注〔2021〕54号 2021.11.04<br>
国家药监局关于印发境内第三类和进口医疗器械注册审批操作规范的通知<br>国药监械注〔2021〕53号 2021.11.04
创新医疗器械特别审查程序<br>2018年第83号<br>
创新医疗器械特别审查申报资料编写指南<br>2018年第127号<br>
关于进口医疗器械注册申请人和备案人名称使用中文的公告<br>2017年第131号<br>
【注册体考】
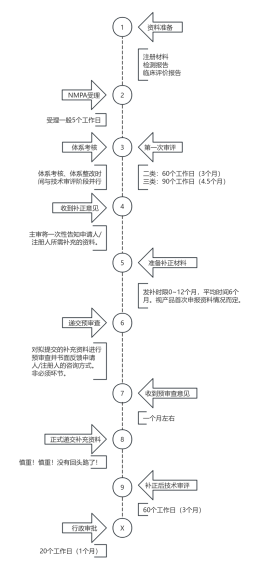
境内第三类医疗器械注册质量管理体系核查工作程序<br>药监综械注〔2022〕13号 2022.02.11<br>
食品药品监管总局关于印发境内第三类医疗器械注册质量管理体系核查工作程序(暂行)的通知<br>食药监械管〔2015〕63号 2015.06.08(已作废)
发布医疗器械注册质量管理体系核查指南的通告<br>(2022年第50号)2022-10-10<br>
excel格式
《医疗器械注册质量管理体系核查指南》<br>2020年 第19号通告 2020.03.10 (已作废)<br>
医疗器械注册质量管理体系核查指南(修订征求意见稿)<br>2022-05-27<br>
【说明书及标签】(含UDI)
《医疗器械说明书和标签管理规定》<br>总局令2014第6号<br>
《体外诊断试剂说明书编写指导原则》<br>2014年 第17号通告<br>
关于体外诊断试剂说明书文字性变更有关问题的通知<br>食药监办械管〔2016〕117号<br>
UDI相关标准
《医疗器械唯一标识系统规则》<br>2019年 第66号公告 2019.10.01执行<br>
《医疗器械唯一标识系统规则》解读
医疗器械唯一标识数据库
YY∕T 1681-2019 医疗器械唯一标识系统基础术语
YY∕T 0466.1-2016 医疗器械 用于医疗器械标签、标记和提供信息的符号 第1部分:通用要求
GB/T 19946-2022 包装 用于发货、运输和收货标签的一维条码和二维条码<br>2023-05-01<br>
GB/T 41977-2022 包装 一维条码和二维条码的标签和直接产品标记<br>2022-10-12<br>
YY∕T 0466.1-2016 医疗器械 用于医疗器械标签、标记和提供信息的符号 第1部分:通用要求<br>
ISO 15223-1-2021 Medical devices-Symbols to be used with information to be supplied by the manufacturer — Part 1 General requirements
IMDRF/UDI WG/N7FINAL:2013 UDI Guidance-Unique Device Identification (UDI) of Medical Devices<br>2013.12.09
GB∕T 16986-2018 商品条码 应用标识符
GS1通用规范
目录
第1-4章
第5章
第6-8章
【注册检验】
医疗器械产品技术要求编写指导原则<br>2022年第8号 2022.02.09<br>
医疗器械产品技术要求编写指导原则<br>2014年第9号(已作废)<br>
《医疗器械注册自检管理规定》<br>2021年第126号公告 2021-10-22<br>
解读
《广东省医疗器械注册自检现场检查指导原则(试行)》(征求意见稿)
山东省医疗器械自检检查指导原则(试行)
北京市医疗器械注册自检质量管理体系现场检查指导原则(试行)<br>2022.05.25
【医疗器械命名】
《医疗器械通用名称命名规则》<br>总局令2015第19号<br>
医疗器械通用名称命名指导原则<br>2019年第99号<br>
NMPA关于发布医用康复器械通用名称命名指导原则等6项指导原则的通告<br>(2021年第48号)2021-07-15<br>
医用康复器械通用名称命名指导原则
中医器械通用名称命名指导原则
放射治疗器械通用名称命名指导原则
医用软件通用名称命名指导原则
呼吸、麻醉和急救器械通用名称命名指导原则
妇产科、辅助生殖和避孕器械通用名称命名指导原则
关于发布有源手术器械通用名称命名指导原则等6项指导原则的通告<br>(2022年第26号)2022-06-02<br>
有源手术器械
物理治疗器械
患者承载器械
眼科器械
注输、护理和防护器械
临床检验器械
【分类目录及分类界定】
关于发布医疗器械分类目录的公告<br>2017年第104号<br>
关于进一步做好医疗器械产品分类界定工作的通知<br>食药监办械〔2013〕36号<br>
医疗器械产品分类界定工作流程<br>食药监办械〔2013〕36号 2013-03-28<br>
人工智能医用软件产品分类界定指导原则<br> (2021年第47号通告)2021-07-01<br>
重组胶原蛋白类医疗产品分类界定原则<br>(2021年第27号通告) 2021-04-13<br>
2022年医疗器械分类界定结果汇总<br>2022-07-13<br>
人工智能医用软件产品分类界定指导原则<br>2021年第47号<br>
关于发布《体外诊断试剂分类规则》的公告<br>(2021年第129号)2021.10.29<br>
关于印发体外诊断试剂分类子目录的通知<br>食药监械管〔2013〕242号 已作废<br>
解读
关于调整《医疗器械分类目录》部分内容的公告<br>(2022年第25号)2022.03.24<br>
第一类医疗器械产品目录<br>2021.12.30
【一类备案】
国家药监局关于第一类医疗器械备案有关事项的公告<br>(2022年第62号)2022-08-11<br>
正文
附件1 第一类医疗器械备案资料要求及说明
附件2 第一类医疗器械备案表(格式)
附件3 第一类医疗器械备案编号告知书
附件4 第一类医疗器械备案信息表和第一类体外诊断试剂备案信息表
附件5 第一类医疗器械备案操作规范
【二类注册】
湖北省
境内第二类医疗器械注册
境内第二类医疗器械注册变更(登记事项)
境内第二类医疗器械注册变更(许可事项)
【立卷】
国家药监局关于发布《医疗器械产品注册项目立卷审查要求》等文件的通告<br>(2022年第40号)2022-08-31<br>
1.医疗器械产品注册项目立卷审查要求
2.医疗器械变更注册项目立卷审查要求
3.医疗器械免临床评价目录对比立卷审查表
4.医疗器械临床评价立卷审查表
5.体外诊断试剂产品注册项目立卷审查要求
6.体外诊断试剂变更注册项目立卷审查要求
7.体外诊断试剂临床评价立卷审查表(非临床试验)
8.体外诊断试剂临床评价立卷审查表(临床试验)
9.医疗器械临床试验审批项目立卷审查要求
10.医疗器械延续注册项目立卷审查要求
11.体外诊断试剂延续注册项目立卷审查要求
【注册技术审查指导原则】
【通用指导原则】
医疗器械注册单元划分指导原则
医疗器械通用名称命名指导原则
医疗器械产品技术要求编写指导原则
医疗器械产品受益-风险评估注册技术审查指导原则
医疗器械安全和性能的基本原则
医疗器械附条件批准上市指导原则
【IVD通用指导原则】
体外诊断试剂分析性能评估(准确度-方法学比对)技术审查指导原则
体外诊断试剂分析性能评估(准确度-回收实验)技术审查指导原则
核酸扩增法检测试剂注册技术审查指导原则
金标类检测试剂注册技术审查指导原则
酶联免疫法检测试剂注册技术审查指导原则
生物芯片类检测试剂注册技术审查指导原则
发光免疫类检测试剂注册技术审查指导原则
体外诊断试剂临床试验技术指导原则
体外诊断试剂说明书编写指导原则
肿瘤个体化治疗相关基因突变检测试剂技术审查指导原则
肿瘤相关突变基因检测试剂(高通量测序法)性能评价通用注册技术审查指导原则
【有源器械】
有源医疗器械使用期限注册技术审查指导原则
【移动医疗器械】
移动医疗器械注册技术审查指导原则
学习笔记
【无源器械】
无源医疗器械产品原材料变化评价指南
【生物相容性和生物安全性研究】
医疗器械已知可沥滤物测定方法验证及确认注册技术审查指导原则
【一次性无菌产品】
一次性使用无菌手术包类产品注册技术审查指导原则
一次性使用输注器具产品注册技术审查指导原则
【植入性医疗器械】
无源植入性骨、关节及口腔硬组织个性化增材制造医疗器械注册技术审查指导原则
无源植入性医疗器械产品注册申报资料指导原则
无源植入性医疗器械货架有效期注册申报资料指导原则
无源植入性医疗器械临床试验审批申报资料编写指导原则
同种异体植入性医疗器械病毒灭活工艺验证技术审查指导原则
动物源性医疗器械注册技术审查指导原则
【含药器械】
含药医疗器械产品注册申报资料撰写指导原则
【罕见病防治医疗器械】
用于罕见病防治医疗器械注册审查指导原则
【软件及网络安全】
医疗器械软件注册审查指导原则<br>(2022年修订版)2022年第9号<br>2022.03.07<br>
医疗器械软件注册技术审查指导原则<br>(2015年第50号)2015.08<br>
独立软件产品技术要求模板
YY 0775-2010 远距离放射治疗计划系统 高能X(γ)射束剂量计算准确性要求和试验方法
YY/T 0887-2013 放射性粒籽植入治疗计划系统剂量计算要求和试验方法
YY/T 0889-2013 调强放射治疗计划系统 性能和试验方法
YY/T 0973-2016 自动控制式近距离治疗后装设备放射治疗计划系统 性能和试验方法
YY 0709-2009 医用电气设备 第1-8部分:基本安全和基本性能的通用要求并列标准:<br>通用要求 医用电气设备和医用电气系统中报警系统的测试和指南<br>
YY 0637-2013 医用电气设备 放射治疗计划系统的安全要求
YY 0721-2009 医用电气设备 放射治疗记录与验证系统的安全
医疗器械软件技术审查指导原则<br>(第二版征求意见稿)<br>
北京局:医疗软件产品技术审评规范(2017版)
医疗器械人因设计技术审查指导原则 (征求意见稿)
软件更新类型
医学图像存储传输软件(PACS)注册技术审查指导原则<br>2016.03
【网络安全】
【网络安全相关法律法规】
医疗器械网络安全注册审查指导原则<br>(2022年修订版)2022年第7号<br>2022.03.07<br>
北京局:医疗器械网络安全注册审查指导原则实施指南<br>2021.06.03<br>
医疗器械网络安全注册技术审查指导原则<br>2017.01.20
医疗器械网络安全技术审查指导原则<br>(第二版)征求意见稿<br>
【AI】
深度学习辅助决策医疗器械软件审评要点<br>2019.07
人工智能医疗器械注册审查指导原则<br>2022年第8号2022.03.07<br>
人工智能医疗器械注册审查指导原则<br>(征求意见稿)<br>
【学习笔记】
学习笔记.pdf
人工智能医疗器械 肺部影像辅助分析软件 算法性能测试方法<br>(征求意见稿)2021.08.02<br>
肺结节CT图像辅助检测软件注册审查指导原则<br>(2022年第21号)2022-05-26<br>
糖尿病视网膜病变眼底图像辅助诊断软件注册审查指导原则<br>(2022年第23号)2022-06-02<br>
《人工智能医疗器械创新合作平台》
肺炎CT影像AI标准数据库质量手册
糖尿病视网膜病变常规眼底彩色照相AI标准数据库质量手册
医疗人工智能测评公共服务平台和测试技术文稿说明手册
肺炎CT影像辅助分诊与评估软件审评要点(试行)<br>2020.03.05
医学影像云应用及网络安全能力评估白皮书-Tencent
【CMDE指导原则目录】
【普通医疗器械】部分
【体外诊断试剂IVD】部分
【临床评价】
《免于临床评价医疗器械目录》2021版<br>(2021年第71号)2021-09-16<br>
【临床评价推荐路径】
关于发布《医疗器械分类目录》子目录01、04、07、08、09、10、19、21相关产品临床评价推荐路径的通告<br>(2022年第30号)2022-07-14<br>
01“有源手术器械”
04“骨科手术器械”
07“医用诊察和监护器械”
08“呼吸、麻醉和急救器械”
09“物理治疗器械”
10“输血、透析和体外循环器械”
19“医用康复器械”
21“医用软件”
关于发布《医疗器械分类目录》子目录02、03、05、06、16、18、20相关产品临床评价推荐路径的通告<br>(2022年第24号)2022-06-16<br>
02“无源手术器械”
03“神经和心血管手术器械”
05“放射治疗器械”
06“医用成像器械”
16“眼科器械”
18“妇产科、辅助生殖和避孕器械”
20“中医器械”
关于发布《医疗器械分类目录》子目录11、12、13、14、15、17、22相关产品临床评价推荐路径的通告<br>(2022年第20号)2022-05-19<br>
11“医疗器械消毒灭菌器械”
12“有源医疗器械”
13“无源医疗器械”
14“注输、护理和防护器械”
15“患者承载器械”
17“口腔科器械"
22“临床检验器械”
【动物试验】
国家药监局关于发布医疗器械动物试验研究注册审查指导原则 第一部分:决策原则(2021年修订版)<br>等2项注册审查指导原则的通告(2021年第75号)2021.09.18<br>
解读
第一部分:决策原则
第二部分:试验设计、实施质量保证
真实世界数据用于医疗器械临床评价技术指导原则(试行)<br>(2020年第77号)2020.11.26<br>
国家药监局关于发布医疗器械临床评价技术指导原则等5项技术指导原则的通告<br>(2021年第73号)2021.09.18<br>
附件1:医疗器械临床评价技术指导原则
第一部分:主要定义和概念
第二部分:临床评价
1论证申报产品与对比器械广泛相似性的考虑事项
2文献检索报告的参考格式
3文献检索报告中文献选择方法
4境外临床数据可用性的考虑事项
5建立数据评价标准的考虑因素
6参考评估方法
第三部分:临床试验
附件2:决策是否开展医疗器械临床试验技术指导原则
附件3:医疗器械临床评价等同性论证技术指导原则
附件4:医疗器械注册申报临床评价报告技术指导原则
附件5:列入免于临床评价医疗器械目录产品对比说明技术指导原则
【临床试验】
临床试验机构查询
《医疗器械临床试验质量管理规范》<br>总局 卫计委令 第25号<br>
关于医疗器械临床试验备案有关事宜的公告<br>2015年第87号<br>
关于发布《医疗器械临床试验质量管理规范》的公告<br>2022年第28号公告 2022-03-31<br>
国家药监局关于实施《医疗器械临床试验质量管理规范》有关事项的通告<br>2022年第21号2022-03-31<br>
附件:1.医疗器械临床试验方案范本
附件:2.医疗器械临床试验报告范本
附件:3.体外诊断试剂临床试验方案范本
附件:4.体外诊断试剂临床试验报告范本
附件:5.医疗器械/体外诊断试剂临床试验严重不良事件报告表范本
附件6:6.医疗器械/体外诊断试剂临床试验基本文件目录
《医疗器械临床试验质量管理规范》解读
《医疗器械临床试验机构条件和备案管理办法》<br>2017年第145号公告<br>
关于做好医疗器械临床试验机构备案工作的通知<br>食药监办械管〔2017〕161号<br>
医疗器械临床试验设计指导原则
接受医疗器械境外临床试验数据技术指导原则
关于发布医疗器械临床试验数据递交要求等2项注册审查指导原则的通告<br>2021年第91号 2021.11.25<br>
医疗器械临床试验数据递交要求注册审查指导原则
体外诊断试剂临床试验数据递交要求注册审查指导原则
【需/免临床试验目录】
关于发布免于进行临床试验医疗器械目录(第二批修订)的通告<br>2021年第3号通告 2021.01.14<br>
关于发布需进行临床试验审批的第三类医疗器械目录(2020年修订版)的通告<br>2020年第61号通告 2020.09.18<br>
【体外诊断试剂】
《体外诊断试剂注册与备案管理办法》<br>国家市场监督管理总局令第48号2021.10.01施行<br>
关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告<br>(2021年第122号)2022.01.01执行<br>
中华人民共和国医疗器械注册证(体外诊断试剂)(格式)
中华人民共和国医疗器械变更注册(备案)文件(体外诊断试剂)(格式)
医疗器械注册申报资料和批准证明文件格式要求(体外诊断试剂)
体外诊断试剂注册申报资料要求及说明
体外诊断试剂延续注册申报资料要求及说明
体外诊断试剂变更备案/变更注册申报资料要求及说明
变更备案
变更注册
体外诊断试剂安全和性能基本原则清单
国家药监局关于发布体外诊断试剂临床试验技术指导原则的通告<br>(2021年第72号)2021.09.16<br>
关于体外诊断试剂临床试验机构盖章有关事宜的公告<br>第154号公告<br>
《免于临床试验体外诊断试剂目录》2021版<br>(2021年第70号)2021-09-16<br>
【上市后监管】
医疗器械生产监督管理办法<br>总局令第53号 2022.05.01施行<br>
《医疗器械生产监督管理办法》<br>总局令2014年第7号<br>
关于实施《医疗器械生产监督管理办法》《医疗器械经营监督管理办法》有关事项的通告<br>(2022年第18号) 2022.3.11<br>
附件1:医疗器械生产许可申请表及许可证样式
附件2:第一类医疗器械生产备案表及备案凭证样式
附件3:医疗器械经营许可申请表及许可证样式
附件4:第二类医疗器械经营备案表及备案凭证样式
附件5:有关填写说明
禁止委托生产医疗器械目录
关于发布禁止委托生产医疗器械目录的通告<br>2014年第18号<br>
《禁止委托生产医疗器械目录(征求意见稿)》<br>2021.11.19<br>
国家药监局关于发布禁止委托生产医疗器械目录的通告<br>(2022年第17号) 2022.03.24<br>
《医疗器械生产质量管理规范》<br>2014年第64号公告<br>
关于《规范》的实施
关于医疗器械生产质量管理规范执行有关事宜的通告<br>2014年第15号<br>
关于第三类医疗器械生产企业实施医疗器械生产质量管理规范有关事宜的通告<br>2016年第19号<br>
医疗器械生产质量管理规范现场检查指导原则等4个指导原则的通知<br>食药监械监〔2015〕218号<br>
检查指导原则 普通医疗器械
excel格式
相关知识点扩展
无菌相关标准
YY∕T 1244-2014 体外诊断试剂用水
YY∕T 1759-2020 医疗器械软性初包装设计与评价指南
关于文件管理
GB/T 41597-2022 质量管理 文化和机制支撑服务提升指南<br>2022-10-12<br>
关于批及批记录
GB/T 19892.4-2022 批控制 第 4 部分:批生产记录<br>2023-05-01
《医疗器械生产质量管理规范 附录无菌医疗器械》<br>2015年第101号<br>
检查指导原则 无菌医疗器械
GB/T 14233.1-2022 医用输液、输血、注射器具检验方法 第 1 部分:化学分析方法<br>2023-11-01<br>
《医疗器械生产质量管理规范 附录植入性医疗器械》<br>2015年第102号<br>
检查指导原则 植入性医疗器械
《医疗器械生产质量管理规范 附录体外诊断试剂》<br>2015年第103号<br>
检查指导原则 体外诊断试剂
《医疗器械生产质量管理规范 附录定制式义齿》<br>2016年第195号<br>
医疗器械生产质量管理规范定制式义齿现场检查指导原则<br>食药监械监〔2016〕165号<br>
《医疗器械生产质量管理规范 附录独立软件》<br>2019年 第43号<br>
医疗器械生产质量管理规范独立软件现场检查指导原则<br>药监综械管〔2020〕57号<br>
excel格式
学习笔记
相关知识点扩展
《数据中心设计规范》<br>GB 50174-2017<br>
YY∕T 0664-2020 医疗器械软件 软件生存周期过程
to术语
4-9章正文
附录A本标准要求的理由说明
附录B关于本标准条款的指南
附录C与其他标准的关系
附录D实施
GB/T 8566-2022 系统与软件工程 软件生存周期过程<br>2023-05-01
GB/T 28827.1-2022 信息技术服务 运行维护 第 1 部分:通用要求<br>2023-05-01
IEC 62304:2015 Medical device software-Software life cycle processes
YY∕T 1406.1-2016 医疗器械软件 第1部份 YY∕T 0316 应用于医疗器械软件的指南
GB∕T 25000.51-2016 系统与软件工程 系统与软件质量要求和评价(SQuaRE) 第51部分:就绪可用软件产品(RUSP)的质量要求和测试细则.pdf
笔记
ISO∕IEC∕IEEE 12207-2017 Systems and software engineering Software life cycle processes
国外标准和指南
Content of Premarket Submissions for Device Software Functions<br>器械软件功能的上市前提交内容<br>
DICOM标准
WS 538-2017 医学数字影像通信基本数据集
WS/T 544-2017 医学数字影像中文封装与通信规范
GB/T 41867-2022 信息技术 人工智能 术语<br>2023-05-01<br>
GB/T 41817-2022 信息安全技术 个人信息安全工程指南<br>2023-05-01
GB/T 41905-2022 软件与系统工程 软件测试工具能力<br>2023-05-01
指南性文件
【关于管理者代表】
医疗器械生产企业管理者代表管理指南<br>2018年第96号<br>
重庆
关于上报我市医疗器械生产企业管理者代表相关信息的通知
上海
关于医疗器械生产企业管理者代表登记报备实施全程网办相关事宜的通知
上海市医疗器械生产企业管理者代表责任制实施办法
广东
广东省食品药品监督管理局关于医疗器械企业管理者代表的管理办法
医疗器械生产企业供应商审核指南<br>2015年第1号<br>
医疗器械工艺用水质量管理指南<br>2016年第14号<br>
医疗器械冷链(运输、贮存)管理指南<br>2016年第154号<br>
医疗器械生产企业质量控制与成品放行指南<br>2016年第173号<br>
成品放行前至少应当符合以下条件:
关于发布医疗器械质量管理体系年度自查报告编写指南的通告<br>(2022年第13号)2022.02.24<br>
医疗器械质量管理体系年度自查报告编写指南<br>征求意见稿<br>
医疗器械质量管理体系年度自查报告编写指南
医疗器械生产环节风险清单和检查要点
一次性使用无菌注射器等25种医疗器械生产环节风险清单和检查要点<br>食药监械监〔2016〕37号<br>
一次性使用塑料血袋等21种医疗器械生产环节风险清单和检查要点<br>食药监械监〔2017〕14号<br>
定制式医疗器械监督管理规定(试行)<br>2019年 第53号公告<br>
【关于注册人制度】
关于发布医疗器械委托生产质量协议编制指南的通告<br>(2022年第20号)2022.03.24<br>
国家药监局关于扩大医疗器械注册人制度试点工作的通知<br>国药监械注〔2019〕33号<br>
湖北省
《湖北省医疗器械注册人制度试点工作实施指南(试行)》
《湖北省医疗器械注册人委托生产质量管理体系实施指南(试行)》
长三角
长江三角洲区域医疗器械注册人制度试点工作实施方案<br>2019年10月29日<br>
长江三角洲区域医疗器械注册人制度跨区域监管办法(试行)<br>2020年03月10日
北京市
北京市医疗器械注册人制度试点工作实施方案<br>通告〔2019〕8号2019年12月16日-2021年12月15日<br>
《北京市医疗器械注册人制度试点工作实施方案》政策问答
四川省
关于印发《四川省医疗器械注册人制度试点工作实施方案》的通知<br>川药监发〔2019〕127号2019年11月01日<br>
征求意见稿
【关于监管体系】
国家药监局综合司关于加强医疗器械生产经营分级监管工作的指导意见<br>药监综械管〔2022〕78号 2022-09-09<br>
《医疗器械生产企业分类分级监督管理规定》<br>食药监械监〔2014〕234 号<br>
湖北省医疗器械经营企业分类分级监督管理实施办法(试行)<br>鄂食药监文【2016】70号<br>
附件1:医疗器械生产重点监管品种目录
附件2:医疗器械经营重点监管品种目录
关于境内医疗器械生产企业跨省新开办企业时办理产品注册及生产许可有关事宜的公告<br>2015年第203号<br>
关于印发国家重点监管医疗器械目录的通知<br>食药监械监〔2014〕235号<br>
关于印发湖北省级重点监管医疗器械目录的通知
关于落实食品药品违法行为举报奖励办法有关事项的通知<br>食药监办稽〔2017〕125号<br>
关于加大食品药品安全执法力度严格落实食品药品违法行为处罚到人的规定<br>食药监法〔2018〕12号<br>
【经营及销售】
《医疗器械网络销售监督管理办法》<br>总局令2017第 38 号<br>
《医疗器械网络销售监督管理办法》解读
关于实施《医疗器械网络销售监督管理办法》有关事项的通知<br>食药监办械监〔2018〕31号<br>
医疗器械经营监督管理办法<br>总局令第54号 2022.05.01施行<br>
《医疗器械经营监督管理办法》<br>总局令2014第8号 已作废<br>
关于实施《医疗器械生产监督管理办法》《医疗器械经营监督管理办法》有关事项的通告(2022年第18号)
医疗器械经营质量管理规范<br>2014年第58号公告
国家药监局综合司公开征求《医疗器械经营质量管理规范附录:第三方物流质量管理(征求意见稿)》意见<br>2022年6月10日<br>
《医疗器械广告审查发布标准》<br>局令2009第 40 号<br>
《医疗器械广告审查办法》<br>局令2009第 65 号<br>
《医疗器械使用质量监督管理办法》<br>总局令2015第18号<br>
【自查、飞检、不良事件与召回】
关于发布医疗器械质量管理体系年度自查报告编写指南的通告(2022年第13号)
医疗器械生产企业质量管理体系年度自查报告编写指南<br>2016年第76号 已作废<br>
医疗器械质量管理体系年度自查报告编写指南
《药品医疗器械飞行检查办法》<br>总局令2015第 14 号<br>
关于《药品医疗器械飞行检查办法》的说明
《医疗器械不良事件监测和再评价管理办法》<br>总局令2018第1号<br>
《医疗器械不良事件监测和再评价管理办法》解读
关于贯彻实施《医疗器械不良事件监测和再评价管理办法》有关事项的通知<br>药监综械管〔2018〕35号<br>
关于进一步加强医疗器械不良事件监测体系建设的指导意见<br>食药监械监〔2013〕205号<br>
关于发布医疗器械定期风险评价报告撰写规范的通告<br>2020年第46号通告<br>
医疗器械注册人开展不良事件监测工作指南<br>2020年第25号通告<br>
国家药监局综合司关于印发医疗器械注册人备案人开展不良事件监测工作检查要点的通知<br>药监综械管〔2021〕43号<br>
《医疗器械不良事件监测和再评价管理办法(修正案草案)》(征求意见稿)<br>公开征求意见 2021.11.23
医疗器械注册人开展产品不良事件风险评价指导原则<br>2020.11.27<br>
《医疗器械召回管理办法》<br>总局令2017第29号<br>
《医疗器械召回管理办法》解读一
《医疗器械召回管理办法》解读二
关于实施《医疗器械召回管理办法》有关事项的通知
医疗器械召回事件报告表
医疗器械主动召回信息发布模板
医疗器械责令召回信息发布模板
召回计划实施情况报告表
责令召回通知书
总局政府网站信息采集接口标准规范
关于进一步做好医疗器械召回信息公开工作的通知<br>食药监办械监〔2014〕107号<br>
ISO TR 20416-2020 Medical devices — Post-market surveillance for manufacturers
正文
Annex A数据来源源举例 B分析方法举例
Annex C PMS计划举例
《医疗器械标准管理办法》<br>总局令第33号<br>
医疗器械标准目录汇编<br>2021.11.06更新
《医疗器械标准管理办法》解读之一
《医疗器械标准管理办法》解读之二
医疗器械标准制修订工作管理规范<br>2017年第156号公告<br>
常用标准
GB∕T 19000-2016 质量管理体系 基础和术语
GB/T 20001.11-2022 标准编写规则 第 11 部分:管理体系标准<br>2023-05-01<br>
GB∕T 19001-2016 质量管理体系 要求
GB∕T 19011-2013 管理体系审核指南
GB 9706.1-2020 医用电气设备 第1部分:基本安全和基本性能的通用要求<br>Medical electrical equipment—Part 1: General requirements for basic safety and essential performance<br>2023-05-01<br>
学习资料
YY∕T 0287-2017 医疗器械 质量管理体系用于法规的要求
YY∕T 0595-2020 医疗器械 质量管理体系 YYT 0287-2017应用指南
1-6章
7-8章
BS EN ISO 13485-2016+A11-2021
结合MDR法规的要求
ISO 13485:2016
GB/T 42061-2022 医疗器械 质量管理体系 用于法规的要求<br>2023-11-01<br>
YY∕T 0316-2016 医疗器械风险管理对医疗器械的应用
ISO 14971-2019 Medical devices - Application of risk management to medical devices
学习笔记
YY∕T 0316-2008 医疗器械风险管理对医疗器械的应用
GB/T 42062-2022 医疗器械 风险管理对医疗器械的应用<br>2023-11-01
国外法规要求
欧盟CE
MDR : REGULATION (EU) 2017/745
MDR : REGULATION (EU) 2017/745 中文版
IVDR : REGULATION (EU) 2017/746
IVDR : REGULATION (EU) 2017/746 中文版
REGULATION (EC) 765/2008 与产品营销相关的认证和市场监督要求
中文翻译稿
31985L0374:85/374/EEC
MDCG 2019-11 Guidance on Qualification and Classification of Software in Regulation (EU) 2017/745 – MDR and Regulation (EU) 2017/746 – IVDR
Clinical evaluation under EU MDR -From BSI

Collect
Get Started

Collect
Get Started
Collect
Get Started

Collect
Get Started
评论
0 条评论
下一页





