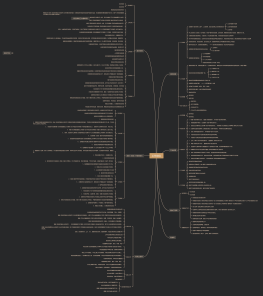
监查员职责
2021-07-29 09:31:32 0 举报
AI智能生成
2020新版GCP中监查员(CRA)的职责
模板推荐
作者其他创作
大纲/内容
0 条评论
下一页