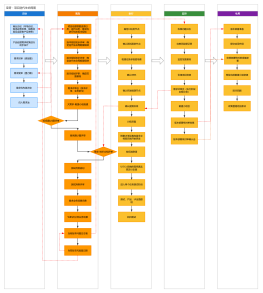
清洁验证生命周期介绍
2024-06-14 15:25:30 0 举报
AI智能生成
制药行业清洁验证生命周期介绍思维导图
模板推荐
作者其他创作
大纲/内容
0 条评论
下一页