有机化学
2023-05-02 12:32:58 0 举报
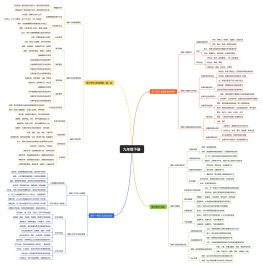
高中选择性必修三有机化学第一二单元概要
模板推荐
作者其他创作
大纲/内容
0 条评论
下一页